![対象児をRSウイルス感染症から守る ベイフォータス(R)使用に関する「コンセンサスガイドラインQ&A(第3版)]改訂の背景と要点](../images/rsv_zadankai5/mv-top.jpg)
更新日:2025年12月10日
日本小児科学会は、妊婦向けのRSウイルス⺟⼦免疫ワクチン接種後の対応について、⺟⼦免疫ワクチン接種にかかわらず、リスクのある新生児に対して抗RSウイルスヒトモノクローナル抗体(抗体薬)の投与を推奨しています。「日本におけるニルセビマブの使用に関するコンセンサスガイドラインQ&A(第3版)」(以下「Q&A(第3版)」)の「3」でもこの推奨を継続し、リスクのあるお子さんをしっかり守るという姿勢をより明確にするため、情報の順列を見直しました。
日本産科婦人科学会による「RSウイルス母子免疫ワクチン(アブリスボ®筋注用)を接種した妊婦への注意点」の改訂も行われました1)。この改訂により「新生児や乳児のリスクに応じて小児科医が抗体薬投与を検討する場合がある」という一文が加えられました。ハイリスク児に対して、妊婦接種後も抗体薬の投与を推奨する考え方は、英国のGreen Book2)やカナダ・ブリティッシュコロンビア州のガイドライン3)でも採用されており、国際的にも整合性のとれた対応と考えています。
現在、妊娠中のRSウイルス母子免疫ワクチン接種に関する情報を、産婦人科と小児科の間で共有できるように、接種後は母子手帳へ接種シールを貼付することをルール化しています。
以下の場合は、妊婦への組換えRSウイルスワクチンの接種にかかわらず、ニルセビマブまたはパリビズマブ投与が推奨されます1)。
なお、以下の場合、特に母体RSウイルスワクチン接種の児に対する効果が低下することが予測され、上記ニルセビマブまたはパリビズマブの適応児には、積極的な投与が推奨されます。
妊娠中に組換えRSウイルスワクチンを接種したかどうか、接種した場合はその接種時期を確認する必要があります。妊娠中に組換えRSウイルスワクチンを接種した場合は、接種年月日がわかるように母子健康手帳に記載しておいてもらうことが大切です。記載がない場合は、接種医療機関に確認するか、母親に接種年月日を確認してもらう必要があります。
1) The green book, chapter 27a: Respiratory syncytial virus. p.11 https://assets.publishing.service.gov.uk/media/669a5e37ab418ab05559290d/Green-book-chapter-27a-RSV-18_7_24.pdf (参照2025-6-30)
2) ベイフォータス®添付文書 https://pins.japic.or.jp/pdf/newPINS/00071367.pdf (参照2025-7-28)
3) シナジス®添付文書 https://www.info.pmda.go.jp/go/pack/6250404A1020_3_03/ (参照2025-7-28)
ベイフォータス®の有効期間は、添付文書に記載があるとおり、MELODY試験およびMEDLEY試験に基づき「少なくとも5か月」とされています4)。この期間については、現在もエビデンスが集積されているところですが、最新のデータとしては、欧州3カ国で実施された実臨床研究HARMONIE試験の追加解析があります5)。これによると、ベイフォータス®投与群は無投与群に比べ、180日間(約6か月)にわたりRSウイルス関連下気道感染による入院が有意に少ないことが示されました。この結果を受け、European Medicines Agencyはベイフォータス®のProduct Informationに記載された有効期間を「少なくとも5〜6か月」に改訂しています6)。日本もこれに準拠し「Q&A(第3版)」の「7」でも、「臨床上『少なくとも5〜6か月間持続』すると考えられる」と表記しました。
ベイフォータス®の有効期間は、後述する流行が通年性と考えられる地域において、投与間隔を考慮するときの一つの指標となります。引き続き最新の情報を注視していく必要があります。
現在入手可能なエビデンスとして、ニルセビマブの国際共同試験の結果から1回の投与で少なくとも5か月間の有効性が示されています(海外後期第Ⅱ相試験(D5290C00003試験)、国際共同第Ⅲ相試験(D5290C00004[MELODY試験])、国際共同第Ⅱ/Ⅲ相試験(D5290C00005[MEDLEY試験])等、「日本におけるニルセビマブの使用に関するコンセンサスガイドライン」参照4))。ただし、5か月以降に全く有効性が期待出来なくなる訳では無く補完データからはある程度の効果の持続は期待されます5)。また、ハイリスク児以外を対象としたニルセビマブの国際共同試験(MELODY試験ならびにHARMONIE試験)について、更に観察期間を180日以上延長した追加解析がなされており、より長期の有効性が検討されています6,7)。よって、臨床上では、前回の投与の効果は、「少なくとも5〜6か月間持続」していると考えられます8)。
一方で150日間未満の観察期間での有効性は比較的高かったが観察期間の延長とともに有効性の低下がみられたとするメタアナリシスもあります9)。長期の効果についてエビデンスが蓄積されてきてはいますが、特にハイリスク児に対する有効期間についてはまだ十分な臨床エビデンスがあるとは言い難い状況です。
4) 日本小児科学会予防接種・感染症対策委員会. 日本におけるニルセビマブの使用に関するコンセンサスガイドライン.
https://www.jpeds.or.jp/modules/activity/index.php?content_id=587 (参照2024-8-5)
5) AstraZeneca & Sanofi June 8, 2023 Meeting of the Antimicrobial Drugs Advisory Committee: Event Materials
https://www.fda.gov/media/169323/download (参照2025-7-28)
6) Arbetter D, et al. Lower Respiratory Tract Infections Following Respiratory Syncytial Virus Monoclonal Antibody Nirsevimab Immunization Versus Placebo: Analysis From a Phase 3 Randomized Clinical Trial(MELODY). Clin Infect Dis. 2024. ciae596.
7) Munro APS, et al. 180-day efficacy of nirsevimab against hospitalisation for respiratory syncytial virus lower respiratory tract infections in infants(HARMONIE): a randomised, controlled, phase 3b trial. Lancet Child Adolesc Health. 2025; 9(6): 404-412.
8) Committee for Medicinal Products for Human Use(CHMP)
https://www.ema.europa.eu/en/committees/committee-medicinal-products-human-use-chmp?utm_source (参照2025-8-22)
9) Ricco M, et al. Impact of Nirsevimab Immunization on Pediatric Hospitalization Rates: A Systematic Review and Meta-Analysis(2024). Vaccines(Basel). 2024; 12(6): 640.
ベイフォータス®は、添付文書の「効能・効果」に記載されているように「生後初回又は2回目のRSウイルス感染流行期」に投与することになっています4)。しかし近年、RSウイルス感染症の流行パターンは大きく変化しており、従来は季節性が明確だった地域でも、流行開始時期が年によって異なったり、収束後まもなく次の流行が始まったりする地域も増えています。
こうした状況を踏まえ、「Q&A(第3版)」では新たに「12-1」を設け、流行の予測が難しい地域においても通年性の考え方を取り入れ、退院時に1回目のベイフォータス®を投与できるようにしました。これにより、生後退院直後の重症化しやすい時期の児をRSウイルス感染症から守ることができます。
2回目の投与時期については、同じ流行シーズンに2回投与することはできないため、次の流行シーズンが始まったときに、先述したベイフォータス®の有効期間「少なくとも5〜6か月」を考慮して判断します。生後2回目の流行期の詳細については、「12-2」をご参照ください。
ニルセビマブの5〜6か月を超える期間の有効性についてはエビデンスの集積中であり14,15,16)、いまだ臨床的には確立されていません。流行期にあわせて投与することで有効性や費用対効果が高くなることが報告されていますので17,18,19,20)、添付文書に沿って流行期にニルセビマブを投与することは重要です。
一方で、「日本におけるニルセビマブの使用に関するコンセンサスガイドライン」では、「RSウイルス感染流行が通年性の地域では、生後12か月齢までを初回感染流行期」とすることも考慮されるとしています21)。最近の日本では、流行開始時期が年ごとに異なり、収束後まもなく新たな流行が開始することもあり、流行開始を予測するのが難しく、投与が間に合わない児が発生してしまう懸念があります。従って、このような場合も通年性の流行と考えてニルセビマブを生後退院時等に投与することは、特に重症化しやすい早期乳児期に予防できるメリットがあり、選択肢と考えられます。地域の流行状況や特性なども踏まえて判断し、健康保険の審査員等との情報共有をすることも重要です。
14) Arbetter D, et al. Lower Respiratory Tract Infections Following Respiratory Syncytial Virus Monoclonal Antibody Nirsevimab Immunization Versus Placebo: Analysis From a Phase 3 Randomized Clinical Trial(MELODY). Clin Infect Dis. 2024. ciae596.
15) Munro APS, et al. 180-day efficacy of nirsevimab against hospitalisation for respiratory syncytial virus lower respiratory tract infections in infants(HARMONIE): a randomised, controlled, phase 3b trial. Lancet Child Adolesc Health. 2025; 9(6): 404-412.
16) Committee for Medicinal Products for Human Use(CHMP)
https://www.ema.europa.eu/en/committees/committee-medicinal-products-human-use-chmp?utm_source (参照2025-8-22)
17) Wang Q, et al. Cost-effectiveness analysis of nirsevimab for prevention of respiratory syncytial virus disease among infants in Shanghai, China: A modeling study. Hum Vaccin Immunother. 2025; 21(1): 2506288.
18) Hodgson D, et al. Optimal Respiratory Syncytial Virus intervention programmes using Nirsevimab in England and Wales. Vaccine. 2022; 40(49): 7151-7157.
19) Getaneh AM, et al. Cost-effectiveness of monoclonal antibody and maternal immunization against respiratory syncytial virus(RSV) in infants: Evaluation for six European countries. Vaccine. 2023; 41(9): 1623-1631.
20) Lastrucci V, et al. The impact of nirsevimab prophylaxis on RSV hospitalizations: a real-world cost-benefit analysis in Tuscany, Italy. Front Public Health. 2025; 13: 1604331.
21) 日本小児科学会予防接種・感染症対策委員会. 日本におけるニルセビマブの使用に関するコンセンサスガイドライン.
https://www.jpeds.or.jp/modules/activity/index.php?content_id=587 (参照2024-8-5)
「日本におけるニルセビマブの使用に関するコンセンサスガイドライン」では、「RSウイルス感染流行が通年性の地域では、生後12か月齢までを初回感染流行期、生後12〜24カ月齢を生後2回目の感染流行期とすることも考慮される。」としています22)。また、流行開始時期が変動し予測が難しいために通年性の流行と考えてニルセビマブを生後退院時等に投与した場合、同じ流行シーズンにニルセビマブの2回投与はできませんが、次の流行が始まったと考えられる場合には「生後2回目のRSウイルス感染流行期」と考えて5〜6か月のニルセビマブの有効期間を考慮(Q7参照)したうえで2回目の投与時期を決めることが推奨されます。
22) 日本小児科学会予防接種・感染症対策委員会. 日本におけるニルセビマブの使用に関するコンセンサスガイドライン.
https://www.jpeds.or.jp/modules/activity/index.php?content_id=587 (参照2024-8-5)
RSウイルス感染症は、流行期の開始だけでなく、収束時期の予測も難しいのが現状です。流行期の後半で流行が落ち着いている時期は投与可能ですが、地域で流行期が終了と判断されている場合は、原則投与ができません。その指標として、「Q&A(第3版)」の「8」では、各都道府県の投与ガイダンスに従って投与することを明記しました。また、対象児への投与漏れ防止や予期せぬ流行開始に備えて、日本新生児成育医学会が提供している「抗RSウイルスモノクローナル製剤の適応確認シート」8)の活用も呼びかけています。このシートは、対象児の生年月日や適応症等から、投与可能薬剤や投与可能期間が記されるサポートツールです。現在は「ニルセビマブの通年性運用適応確認シート」も利用可能となっています(最新NEWS参照)。ぜひご活用ください。
RSウイルス感染症流行期の後半で、流行が落ち着いてきている時期でもニルセビマブの投与は可能です。流行がどのように終息するかや終息する時期の予測は難しいためです。対象児をRSウイルス感染症から予防するために各都道府県の投与ガイダンスに従い、適応児に適切な抗体製剤の投与を行うことが望ましい。対象児への投与漏れ防止や予期せぬ流行開始に備えて抗RSウイルスモノクローナル製剤の適応確認シート(日本新生児成育医学会ホームページ掲載)10)等により投与対象児をリストアップすることも効果的である。
一方、定点あたりの報告数など地域で流行期が終了していると判断する場合は、原則、投与することはできません。
通年性の流行と考えられる場合にはQ12を参照ください。
10) 日本新生児成育医学会. 抗RSウイルスモノクローナル製剤の適応確認シート. https://jsnhd.or.jp/doctor/info/anti-rs-virus_seet.html (参照2025-7-28) (最新NEWS参照)
ベイフォータス®の投与方法は地域に合わせて、次の3つのパターンに分けることができます。
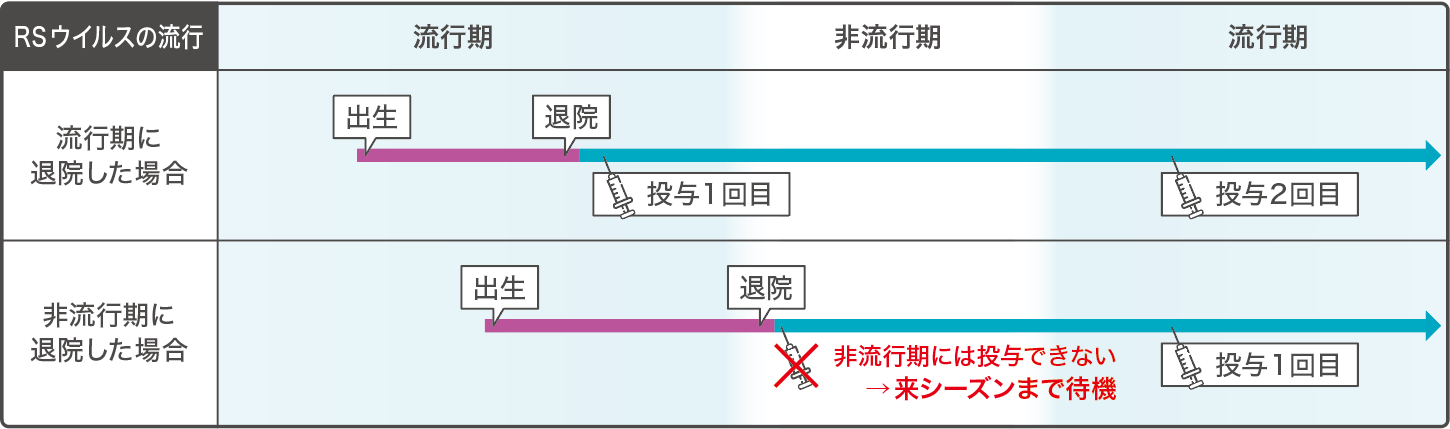
RSウイルス感染症に季節性のある地域の場合、流行期に合わせて投与するので、「退院時」が流行期内であればその期間内にベイフォータス®を投与します。退院時が非流行期であれば、来シーズンまで待機することになります。
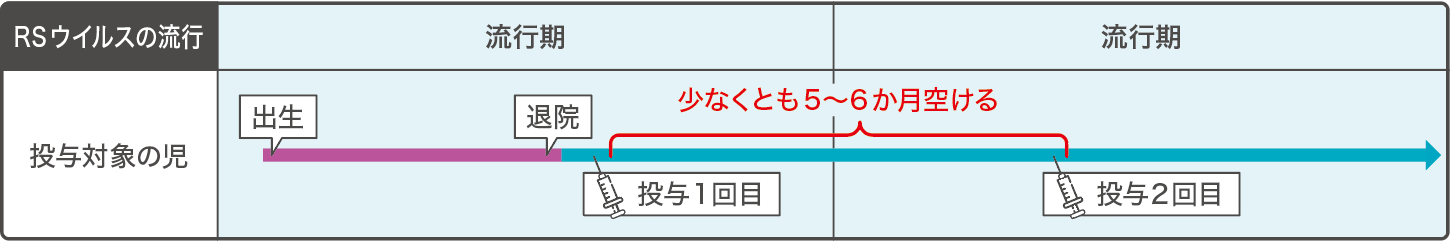
退院時に1回目のベイフォータス®を投与します。同じ流行シーズンに2回投与することはできないため、2回目の投与時期は2回目の流行期開始が確認されたら、ベイフォータス®の有効期間「少なくとも5〜6か月」を考慮して投与時期を判断します。
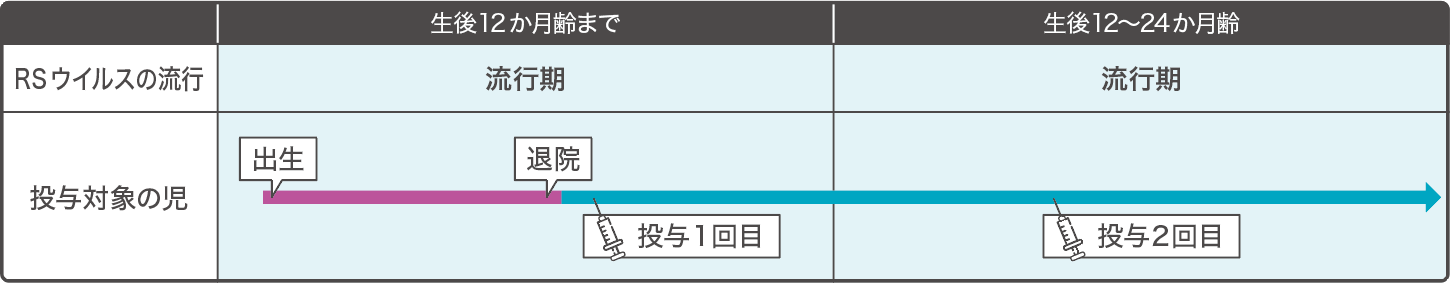
「日本におけるニルセビマブの使用に関するコンセンサスガイドライン」7)に基づき、生後12か月齢までを初回感染流行期、生後12〜24か月齢を生後2回目の感染流行期と捉え、合計2回の投与ができるように投与管理します。
ご施設の地域がどのパターンに該当するかは、都道府県のガイダンスや各地域の流行状況、
保険審査の方針等を踏まえて判断してください。
RSウイルス感染症は、地域ごとに流行パターンや医療体制が異なり、近年は流行時期の見通しがつきにくい状況が続いています。このような現状に対し、長期間作用型の抗体製剤のベイフォータス®が果たすべき役割は大きく、適応を有する対象児には、ベイフォータス®の投与が推奨されます。
リスクのあるお子さんを漏れなくRSウイルス感染症から守る―それが今回の改訂の真の目的です。地域の多様性を考慮し、どの地域でも柔軟に運用しやすいように意図的に幅を持たせた改訂になっています。地域の実情に合わせながら、引き続きベイフォータス®の適正使用を推進してほしいと思います。
2025年10月、日本新生児成育医学会が提供している季節性投与向けの「抗RSウイルスモノクローナル製剤の適応確認シート」に加えて、ベイフォータス®の通年性投与に適した「ニルセビマブの通年性運用適応確認シート」が追加されました8)。これはベイフォータス®対象児の生年月日や適応症、RSウイルス抗体薬の投与歴などを入力すると、ベイフォータス®の2回目以降の投与可能期間や推奨投与時期が示されるサポートツールです。
ベイフォータス®の初回投与は、基本的にNICU退院時であるため確実に投与されますが、2回目以降は外来へ移行したり、転院があったりと、投与管理が難しくなりがちです。各診療科で2回目の投与タイミングについて目線合わせをしたうえで、投与対象児に漏れなく投与するために各診療科、さらには地域全体で同シートを活用し、適切なベイフォータス®の投与管理体制の構築に役立てていただきたいと思います。
1)日本産科婦人科学会. RS ウイルス母子免疫ワクチン(アブリスボ®筋注用)を接種した妊婦への注意点(改定版)
https://www.jsog.or.jp/news/pdf/20250906_kaiin.pdf (参照2025-10-20)
2)The green book, chapter 27a: Respiratory syncytial virus. p.11
https://assets.publishing.service.gov.uk/media/669a5e37ab418ab05559290d/Green-book-chapter-27a-RSV-18_7_24.pdf (参照2025-10-20)
3)BC Infant Respiratory Syncytial Virus(RSV)Immunoprophylaxis Program Questions and Answers for Immunization Providers Updated September 2025 BC Centre for Disease Control. p.8
https://www.bccdc.ca/resource-gallery/Documents/Guidelines%20and%20Forms/Guidelines%20and%20Manuals/Immunization/Vaccine%20Info/RSV_Nirsevimab_HCP_QA.pdf (参照2025-10-20)
4)ベイフォータス®添付文書 https://pins.japic.or.jp/pdf/newPINS/00071367.pdf (参照2025-10-20)
5)Munro APS, et al. Lancet Child Adolesc Health. 2025; 9(6): 404-412.
6)European Medicines Agency. Beyfortus: EPAR–Product information. EMA/VR/0000246848.
https://www.ema.europa.eu/en/medicines/human/epar/beyfortus(参照2025-10-20)
7)日本小児科学会予防接種・感染症対策委員会. 日本におけるニルセビマブの使用に関するコンセンサスガイドライン.
https://www.jpeds.or.jp/modules/activity/index.php?content_id=587 (参照2025-10-20)
8)日本新生児成育医学会. ニルセビマブの通年性運用適応確認シート.
https://jsnhd.or.jp/doctor/info/anti-rs-virus_seet.html(参照2025-10-20)